小药谈肿瘤免疫:CD47-SIRPa轴
前言
固有免疫系统维持着一种完美的平衡,在健康组织中保持静止,而面对致病性刺激时可以迅速激活。巨噬细胞是固有免疫系统的关键效应分子,随时检测着激活和抑制信号,以启动吞噬和分泌细胞因子的功能。
细胞表面蛋白CD47是一种“不要吃我”的信号,它保护健康细胞不被巨噬细胞吞噬,缺乏CD47的造血细胞会被巨噬细胞迅速吞噬并触发树突状细胞的活化。CD47在癌细胞上的表达通常会增加,作为逃避免疫检测的一种机制。CD47的阻断性抗体会抑制肿瘤的生长甚至彻底清除肿瘤。
靶细胞表面的CD47会被巨噬细胞或树突状细胞上的SIRPA(信号调节蛋白?)识别。SIRPA是一种含有多重细胞内基于酪氨酸的免疫抑制基序(ITIMs)的抑制性受体。缺乏SIRPA的巨噬细胞对携带CD47的靶细胞的吞噬作用不明显,这表明SIRPA是CD47信号的主要感受器。SIRPA必须以高度精确的方式来激活,以保证在CD47存在时抑制对活细胞的吞噬,而对缺乏CD47的靶点进行强有力的吞噬。CD47通过Src家族的激酶触发SIRPA磷酸化,磷酸化的SIRPA招募磷酸酶SHP-1和SHP-2,但是CD47如何驱动SIRPA磷酸化以及这些磷酸酶的下游靶点及其与吞噬过程的关系还不清楚。了解CD47-SIRPA抑制吞噬的作用机制对癌症免疫治疗的应用具有重要意义。
CD47抑制IgG和磷脂酰丝氨酸“吃我”信号
为了研究吞噬过程中“吃我”和“不要吃我”信号整合的机制,研究人员使用了一个重组的吞噬靶标。这个靶标是将硅珠包裹在一个支持的脂质双层膜上,以模拟癌细胞的表面。为了激活SIRPA,研究人员将CD47胞外结构域按一定的密度(~600分子/mm2)整合来模拟癌细胞上的CD47。

利用这个系统,测试了CD47对IgG和磷脂酰丝氨酸的吞噬作用。可以发现CD47抑制了中等IgG密度下的吞噬,但对高密度结合IgG的靶标吞噬作用并不明显。CD47的存在并没有完全消除吞噬作用,而是导致开始吞噬的细胞比例和每个细胞被吞噬的小球数量的数量减少。这种抑制依赖于CD47的激活,因为突变的CD47胞外结构域不能与SIRPA结合(F37D,T115K),无法抑制吞噬。另外,含有10%磷脂酰丝氨酸的珠子的吞噬被包含在脂质双层上的CD47抑制。这些数据表明CD47-SIRPA信号可以阻断IgG和磷脂酰丝氨酸驱动的吞噬。CD47使SIRPA重新定位于吞噬突触
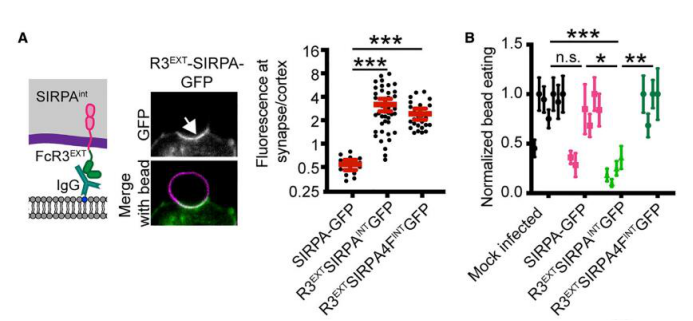
为了确定CD47调节SIRPA活性的机制,研究人员首先检查了SIRPA在IgG包被小球吞噬过程中的定位。当SIRPA不与CD47结合时,SIRPA与包裹IgG包被小球的吞噬杯分离。相反,在CD47的存在下,SIRPA仍停留在吞噬杯中。这些数据表明,未结合的SIRPA被排除在吞噬突触之外,而CD47结合SIRPA后使其仍保留在吞噬突触中。
在IgG和CD47缺失的情况下SIRPA从吞噬杯中分离的机制推测可能是由SIRPA高度糖基化的胞外结构域驱动的。为了验证这个想法,研究人员创建了一个SIRPA嵌合受体,其中胞外域被一个小的惰性蛋白结构域取代(FRBEXTT-SIRPA)。与全长SIRPA不同,FRBEXT-SIRPA没有与细胞靶向突触分离。这一结果表明SIRPA的胞外结构域是将SIRPA排除在吞噬突出之外所必需的。

SIRPA集中在免疫突触抑制吞噬
SIRPA包含两个免疫酪氨酸抑制基序(ITIMs),它们被Src家族激酶磷酸化,对下游信号传递至关重要。因此,可以推测将SIRPA定位在吞噬杯中可能驱动ITIM磷酸化和受体激活。为了区分CD47结合和突触定位的影响,研究人员开发了一种嵌合SIRPA受体,将SIRPA胞外结构域替换为FcgR3a链的IgG结合胞外结构域(FcR3EXT SIRPAINT),在CD47缺失的情况下定位于吞噬突触。这种突触定位嵌合体的表达抑制了IgG包被小球的吞噬。
作为对照,研究人员另外表达了一个嵌合结构,其中ITIM结构域的四个酪氨酸突变为苯丙氨酸,抑制了SIRPA的磷酸化和激活(FcR3ext SIRPA 4Fint)。这种结构不影响吞噬,表明SIRPA嵌合体的抑制作用是信号依赖的。因此,将SIRPA定位到吞噬杯足以抑制吞噬,即使在缺乏其天然配体CD47的情况下。
CD47抑制整合素活化
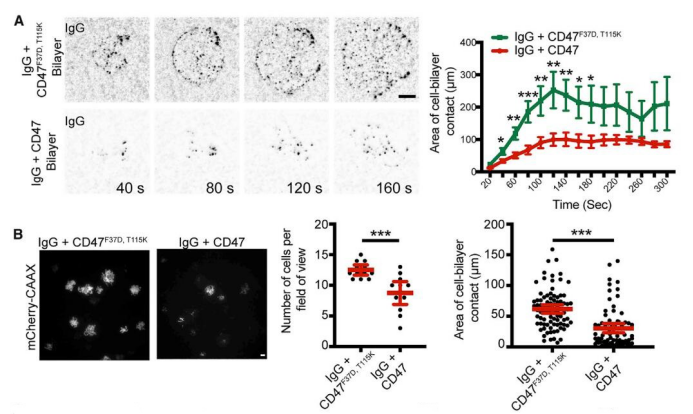
通过观察巨噬细胞登陆脂质双层膜的动力学,可以发现,IgG涂层的双层膜上的细胞遍布双层膜表面。相反,巨噬细胞遇到含有IgG和CD47的双层膜时,细胞扩散减少。静态时间点的TIRF成像显示,与含野生型CD47的双层膜相互作用的巨噬细胞较少,相互作用的巨噬细胞足迹较小。这些数据表明,CD47抑制了巨噬细胞在靶向底物上的扩散。
细胞扩散被认为涉及整合素和肌动蛋白细胞骨架的激活。未激活的整合素以低亲和力、弯曲的形式存在。激活后,整合素的胞外结构域会扩展为开放构象,可结合许多具有高亲和力的配体。FcR激活会刺激整合素的由内而外的活化。激活的整合素可通过增加与靶粒子的粘附力或提供细胞内信号和肌动蛋白组装来促进吞噬。通过用β2整合素功能阻断性抗体或Fab抑制整合素可显著降低IgG介导的吞噬效率。
CD47-SIRPA信号是否是通过抑制整合素由内到外的激活来抑制吞噬呢?为了验证这个想法,科研人员利用锰来处理巨噬细胞,而锰会将整合素锁定为高亲和力的开放构象。
结果发现,无论CD47是否与支持的脂质双层膜结合,用1 mM锰包被的小球处理的巨噬细胞具有相似的效率。重要的是,锰本身不会引发吞噬,也不会在缺乏CD47的情况下显著增强IgG包被小球的吞噬,从而证明增加整合素的活化以引发吞噬。因此,锰引起的吞噬增加对含有CD47和IgG的小球是特异的。
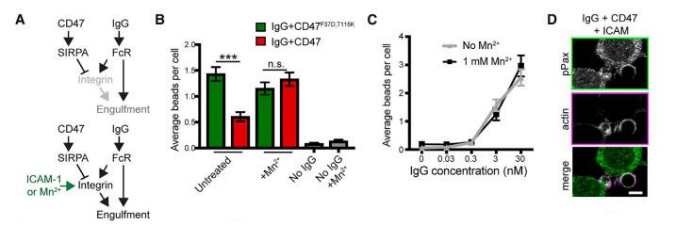
另一方面,通过用含有过量高亲和力整合素配体ICAM-1的小球培养巨噬细胞。即使在CD47存在的情况下,ICAM-1也足以激活整合素,高浓度ICAM-1的加入消除了CD47对吞噬的抑制作用,但在没有CD47的情况下,并没有显著改变IgG包被小球的吞噬效率。尽管存在CD47,但ICAM-1结合的珠子与缺乏CD47的珠子具有相似的肌动蛋白积累水平。这表明激活整合素可以恢复巨噬细胞吞噬的能力。综上所述,这些数据表明整合素的由内而外的激活可能是CD47-SIRPA参与后抑制的主要靶点。

图片新闻
技术文库
最新活动更多
-
7.30-8.1火热报名中>> 全数会2025(第六届)机器人及智能工厂展
-
7月30-31日报名参会>>> 全数会2025中国激光产业高质量发展峰会
-
精彩回顾立即查看>> 【线下论坛】新唐科技2025新品发布会
-
精彩回顾立即查看>> 【在线会议】研华嵌入式核心优势,以Edge AI驱动机器视觉升级
-
精彩回顾立即查看>> OFweek 2025(第十四届)中国机器人产业大会
-
精彩回顾立即查看>> 【在线会议】从直流到高频,材料电特性参数的全面表征与测量







 分享
分享












发表评论
请输入评论内容...
请输入评论/评论长度6~500个字
暂无评论
暂无评论